- CRISPR — технологія, що змінює майбутнє генетики
- Що таке CRISPR простими словами?
- Як бактерії підказали вченим революційну ідею
- Чому CRISPR змінив правила гри
- Де застосовують CRISPR сьогодні
- Медицина: від лабораторії до клініки
- Сільське господарство: їжа майбутнього
- Діагностика захворювань
- Фундаментальна наука
- Нові покоління CRISPR-технологій
- Base editing — редагування окремих «літер» ДНК
- Prime editing — «пошук і заміна» для ДНК
- CRISPRi та CRISPRa — регуляція без розрізання
- Етичні виклики та суспільна дискусія
- Справа Хе Цзянькуя
- Де проходить межа?
- Ризики та обмеження технології
- Нецільові мутації (off-target effects)
- Доставка в клітини
- Мозаїцизм
- CRISPR та біобезпека
- Нобелівська премія та визнання
- Що чекає CRISPR у майбутньому
- Ключові факти про CRISPR
- Чому CRISPR важливий для кожного
CRISPR — технологія, що змінює майбутнє генетики
Уявіть, що ви можете відкрити текстовий файл, знайти помилку в одному слові та виправити її. А тепер уявіть, що цей «файл» — це ДНК живого організму, а «помилка» — мутація, яка спричиняє невиліковну хворобу. Саме це робить CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats) — революційна технологія редагування генів, яка перевернула біологію та медицину.
CRISPR — це не фантастика. Це реальний інструмент, який уже сьогодні використовують тисячі лабораторій по всьому світу. Він дозволяє точно, швидко та відносно дешево змінювати ДНК будь-якого організму — від бактерій до людини. У 2020 році за розробку цієї технології Еммануель Шарпентьє та Дженніфер Дудна отримали Нобелівську премію з хімії.
Ця стаття — ваш перший крок у світ генного редагування. Ми розглянемо, як працює CRISPR, звідки він з’явився, де його застосовують і чому він викликає одночасно захоплення та побоювання.
Що таке CRISPR простими словами?
CRISPR розшифровується як Clustered Regularly Interspaced Short Palindromic Repeats — «короткі паліндромні повтори, регулярно розташовані групами». Ця назва описує особливу структуру в ДНК бактерій, яку вчені виявили ще у 1987 році.
Простіше кажучи, CRISPR — це природна «імунна система» бактерій. Коли бактерія виживає після атаки вірусу, вона зберігає фрагмент вірусної ДНК у своєму геномі. Цей фрагмент стає своєрідним «фотороботом» ворога. Якщо той самий вірус атакує знову, бактерія впізнає його та знищує.
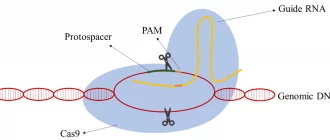
Вчені зрозуміли, що цей механізм можна перетворити на інструмент. Вони створили штучну систему CRISPR/Cas9, де:
- CRISPR — це «навігатор», молекула РНК, яка знаходить потрібну ділянку ДНК
- Cas9 — це «молекулярні ножиці», білок-фермент, який розрізає ДНК у визначеному місці
Після розрізу клітина сама «лагодить» ДНК. У цей момент вчені можуть видалити дефектний ген, вставити новий або замінити одну «літеру» генетичного коду на іншу. Точність цього процесу вражає — система здатна знайти та змінити одну конкретну послідовність серед трьох мільярдів пар нуклеотидів у геномі людини.
Як бактерії підказали вченим революційну ідею
Історія CRISPR — це приклад того, як фундаментальне дослідження непопулярної теми може змінити весь світ. Усе почалося з вивчення імунітету бактерій — теми, яка десятиліттями не привертала широкої уваги.
У 1987 році японський вчений Йосідзумі Ішино випадково клонував незвичайну ділянку ДНК кишкової палички Escherichia coli. Ця ділянка містила повторювані послідовності, розділені унікальними фрагментами. Ніхто тоді не зрозумів, навіщо вони потрібні.
У 2000-х роках іспанський мікробіолог Франсіско Мохіка виявив подібні структури у багатьох видах бактерій та архей. Він запропонував назву CRISPR і висунув гіпотезу, що ці послідовності пов’язані із захистом від вірусів. Його стаття була відхилена кількома журналами — тема здавалася занадто вузькою.
Переломний момент настав у 2007 році. Вчені з компанії Danisco (виробник йогуртів Danone) експериментально довели, що CRISPR дійсно захищає бактерії від вірусів. Це було не просто академічне відкриття — компанія шукала спосіб захистити молочнокислі бактерії від бактеріофагів, які знищували виробництво.
У 2012 році команди Еммануель Шарпентьє та Дженніфер Дудни опублікували в журналі Science статтю, яка змінила все. Вони показали, що систему CRISPR/Cas9 можна запрограмувати на розрізання будь-якої заданої послідовності ДНК. Практично одночасно литовський біохімік Вірджініус Шикшніс з Вільнюського університету отримав аналогічні результати.
На початку 2013 року групи Фена Чжана та Джорджа Черча довели, що CRISPR/Cas9 працює в клітинах людини. Після цього розпочалася справжня революція в генетиці.
Чому CRISPR змінив правила гри
До появи CRISPR вчені вже мали інструменти для редагування генів — нуклеази з «цинковими пальцями» (ZFN) та системи TALEN. Однак ці методи були дорогими, складними та повільними. Для кожної нової «мішені» потрібно було створювати окремий білок, що займало місяці роботи та коштувало десятки тисяч доларів.
CRISPR змінив усе. Ось чому він став проривом:
| Параметр | Попередні методи (ZFN, TALEN) | CRISPR/Cas9 |
|---|---|---|
| Вартість | $5 000 — $10 000 за одну мішень | Від $30 — $50 |
| Час підготовки | Тижні та місяці | Кілька днів |
| Складність | Потрібен окремий білок для кожної мішені | Один білок Cas9 + змінна РНК-послідовність |
| Мультиплексність | Складно редагувати кілька генів одночасно | Можна редагувати кілька генів за один раз |
| Доступність | Лише спеціалізовані лабораторії | Будь-яка молекулярно-біологічна лабораторія |
По суті, CRISPR демократизував генну інженерію. Якщо раніше редагування генів було привілеєм кількох десятків лабораторій у світі, то тепер це доступно практично кожному дослідницькому центру. Кількість наукових публікацій з використанням CRISPR зросла з кількох десятків у 2012 році до десятків тисяч щорічно.
Де застосовують CRISPR сьогодні
Медицина: від лабораторії до клініки
Найбільш очікуване застосування CRISPR — лікування генетичних захворювань. У грудні 2023 року відбулася історична подія: Управління з контролю за продуктами та ліками США (FDA) та Агентство з регулювання лікарських засобів Великої Британії (MHRA) схвалили Casgevy (exa-cel) — перший у світі лікарський препарат на основі CRISPR. Він призначений для лікування серпоподібноклітинної анемії та бета-таласемії — тяжких спадкових захворювань крові.
Принцип дії Casgevy полягає в тому, що у пацієнта відбирають стовбурові клітини крові, редагують їх за допомогою CRISPR і повертають назад в організм. Відредаговані клітини починають виробляти функціональний гемоглобін. Клінічні випробування показали, що у 97% пацієнтів із серпоподібноклітинною анемією зникли больові кризи протягом щонайменше 12 місяців після лікування.
Крім того, CRISPR активно досліджують для боротьби з:
- Онкологічними захворюваннями — редагування імунних клітин (CAR-T терапія) для більш ефективного знищення пухлин
- ВІЛ-інфекцією — видалення вірусної ДНК, інтегрованої в геном людини
- Спадковою сліпотою — перші клінічні випробування in vivo (безпосередньо в організмі) при амаврозі Лебера
Станом на 2025 рік у світі зареєстровано понад 80 клінічних випробувань із застосуванням CRISPR-терапій.
Сільське господарство: їжа майбутнього
CRISPR відкриває нові можливості для створення сільськогосподарських культур, стійких до посухи, хвороб та шкідників. На відміну від традиційних ГМО, CRISPR-модифіковані рослини часто не містять чужорідної ДНК — вчені лише «вимикають» або коригують власні гени рослини.
Приклади вже існуючих CRISPR-модифікованих продуктів:
- Помідори з підвищеним вмістом GABA — амінокислоти, що знижує кров’яний тиск (Японія, 2021)
- Шампіньйони, що не темніють — перший CRISPR-продукт, схвалений у США (2016)
- Пшениця зі зниженим вмістом глютену — для людей із целіакією
У багатьох країнах, включаючи США, Японію, Аргентину та Бразилію, CRISPR-модифіковані організми, що не містять чужорідної ДНК, не підпадають під регулювання ГМО. Це суттєво прискорює їх вихід на ринок.
Діагностика захворювань
CRISPR використовують не лише для редагування генів, а й для їх виявлення. Системи на основі білків Cas12 та Cas13 здатні розпізнавати специфічні послідовності ДНК або РНК з надзвичайною точністю.
Під час пандемії COVID-19 були розроблені CRISPR-діагностичні тести, які визначали наявність вірусу SARS-CoV-2 за 20–40 хвилин без складного лабораторного обладнання. Технологія SHERLOCK (на основі Cas13) та DETECTR (на основі Cas12) можуть стати основою для портативних діагностичних пристроїв нового покоління.
Фундаментальна наука
CRISPR став незамінним інструментом для вивчення функцій генів. Вчені можуть «вимикати» конкретні гени та спостерігати, як це впливає на організм. Це дозволяє розкривати молекулярні механізми захворювань, розвитку та еволюції.
За допомогою CRISPR створено тисячі модельних організмів — від мишей з конкретними мутаціями до генетично модифікованих рептилій та молюсків. Раніше створення таких моделей займало роки, тепер — тижні.
Нові покоління CRISPR-технологій
Технологія не стоїть на місці. Вчені постійно вдосконалюють CRISPR, створюючи більш точні та безпечні інструменти.
Base editing — редагування окремих «літер» ДНК
У 2016 році група Девіда Лю з Гарвардського університету створила base editors — «редактори основ». Ці інструменти можуть замінити одну «літеру» генетичного коду на іншу без розрізання обох ланцюгів ДНК. Це значно безпечніше, ніж класичний CRISPR/Cas9, оскільки зменшує ризик небажаних мутацій.
Близько 60% відомих патогенних мутацій у людини — це заміна однієї нуклеотидної основи. Тому base editing має величезний потенціал для лікування генетичних захворювань.
Prime editing — «пошук і заміна» для ДНК
У 2019 році та сама група Девіда Лю представила ще більш точний інструмент — prime editing. Його порівнюють із функцією «знайти та замінити» у текстовому редакторі. Prime editing може вносити будь-які точкові зміни — вставки, видалення та заміни — без подвійного розриву ДНК та без донорського шаблону.
Теоретично prime editing здатний виправити до 89% відомих генетичних варіантів, пов’язаних із захворюваннями людини.
CRISPRi та CRISPRa — регуляція без розрізання
Не завжди потрібно змінювати ДНК. Іноді достатньо «приглушити» або «підсилити» роботу гена. Для цього створені системи CRISPRi (інтерференція) та CRISPRa (активація). Вони використовують модифікований білок dCas9, який не розрізає ДНК, а лише зв’язується з нею та блокує або стимулює транскрипцію гена.
Ці інструменти особливо цінні для вивчення функцій генів та розробки нових терапевтичних підходів, де потрібно тимчасово змінити активність гена, а не його структуру.
Етичні виклики та суспільна дискусія
Потужність CRISPR породжує серйозні етичні питання. Найгостріша дискусія точиться навколо редагування геному людських ембріонів — змін, які передаватимуться наступним поколінням.
Справа Хе Цзянькуя
У листопаді 2018 року китайський вчений Хе Цзянькуй оголосив про народження перших у світі генетично відредагованих дітей — близнючок Лулу та Нани. Він використав CRISPR для видалення гена CCR5, щоб зробити дівчаток стійкими до ВІЛ-інфекції.
Наукова спільнота засудила цей експеримент. Причини:
- Технологія ще не була достатньо безпечною для клінічного застосування на ембріонах
- Існували альтернативні способи захисту від ВІЛ
- Довгострокові наслідки для здоров’я дітей та їхніх нащадків невідомі
- Експеримент проводився без належного етичного нагляду
Хе Цзянькуй був засуджений до трьох років ув’язнення. Цей випадок прискорив міжнародну дискусію про необхідність чітких правил для редагування геному людини.
Де проходить межа?
Наукова спільнота загалом підтримує використання CRISPR для лікування тяжких генетичних захворювань у соматичних клітинах (клітинах тіла, зміни в яких не передаються нащадкам). Однак щодо редагування зародкових клітин (яйцеклітин, сперматозоїдів та ембріонів) існує фактичний мораторій у більшості країн.
Ключові питання, на які суспільство ще не має однозначних відповідей:
- Чи допустимо редагувати гени ембріонів для запобігання спадковим захворюванням?
- Де межа між лікуванням та «покращенням» людини?
- Хто матиме доступ до генних терапій, якщо вони коштуватимуть мільйони?
- Як запобігти використанню CRISPR для створення «дизайнерських дітей»?
У 2019 році Всесвітня організація охорони здоров’я створила Експертний комітет з питань управління редагуванням геному людини. У 2021 році комітет опублікував рекомендації, які закликають до відповідального використання технології та міжнародного співробітництва у сфері регулювання.
Ризики та обмеження технології
Попри всі переваги, CRISPR не є ідеальним інструментом. Вчені продовжують працювати над вирішенням кількох ключових проблем.
Нецільові мутації (off-target effects)
Система CRISPR/Cas9 іноді розрізає ДНК не лише в потрібному місці, а й у схожих послідовностях. Такі «помилки» називають нецільовими мутаціями. Вони можуть бути нешкідливими, а можуть порушити роботу важливих генів або навіть спровокувати розвиток раку.
Для зменшення цього ризику розроблено модифіковані версії Cas9 з підвищеною точністю — наприклад, eSpCas9 та HiFi Cas9. Нові покоління інструментів, такі як base editing та prime editing, також значно знижують ймовірність нецільових ефектів.
Доставка в клітини
Навіть найточніший інструмент марний, якщо його не можна доставити до потрібних клітин в організмі. Доставка компонентів CRISPR залишається одним із найбільших технічних викликів, особливо для терапії in vivo.
Основні методи доставки включають вірусні вектори (зокрема, адено-асоційовані віруси — AAV), ліпідні наночастинки та електропорацію. Кожен метод має свої обмеження щодо розміру вантажу, ефективності та безпеки.
Мозаїцизм
При редагуванні ембріонів або багатоклітинних організмів CRISPR може спрацювати не в усіх клітинах. У результаті організм стає «мозаїчним» — частина клітин містить відредагований геном, а частина — ні. Це ускладнює терапевтичне застосування та може призвести до непередбачуваних наслідків.
CRISPR та біобезпека
Доступність та простота CRISPR створюють нові виклики для біобезпеки. У 2016 році директор Національної розвідки США Джеймс Клаппер включив редагування генів до переліку потенційних загроз масового знищення.
Основні ризики:
- Біохакінг — ентузіасти-аматори експериментують із CRISPR у домашніх умовах, без належного контролю та знань про безпеку
- Генний драйв — технологія, що дозволяє поширити генетичну модифікацію на всю популяцію дикого виду. Це може бути корисним для боротьби з малярійними комарами, але наслідки для екосистеми непередбачувані
- Потенціал для біозброї — теоретична можливість створення нових патогенів або модифікації існуючих
Міжнародна спільнота працює над створенням регуляторних механізмів, які дозволять використовувати потенціал CRISPR, мінімізуючи ризики зловживань.
Нобелівська премія та визнання
У жовтні 2020 року Нобелівський комітет присудив премію з хімії Еммануель Шарпентьє та Дженніфер Дудні «за розробку методу редагування геному». Це стало визнанням не лише конкретного відкриття, а й цілої нової ери в біології.
Примітно, що це була перша Нобелівська премія з природничих наук, яку отримали виключно жінки. Шарпентьє та Дудна стали лише шостою та сьомою жінками в історії, удостоєними Нобелівської премії з хімії.
Водночас рішення Нобелівського комітету не обійшлося без суперечок. Багато вчених вважають, що внесок Фена Чжана, Вірджініуса Шикшніса, Франсіско Мохіки та інших дослідників також заслуговував на визнання. Патентні суперечки між Каліфорнійським університетом у Берклі (команда Дудни) та Інститутом Broad (команда Чжана) тривали роками і стали одними з найгучніших у сучасній науці.
Що чекає CRISPR у майбутньому
Технологія CRISPR розвивається стрімко. Ось кілька напрямків, які визначатимуть її майбутнє:
Генна терапія нового покоління. Очікується схвалення нових CRISPR-терапій для лікування спадкових захворювань — муковісцидозу, м’язової дистрофії Дюшенна, хвороби Гантінгтона та інших. Компанії Editas Medicine, Intellia Therapeutics та CRISPR Therapeutics проводять десятки клінічних випробувань.
Ксенотрансплантація. За допомогою CRISPR вчені редагують геном свиней, щоб їхні органи можна було пересаджувати людям. У 2022 році було проведено першу трансплантацію серця свині людині. Хоча пацієнт прожив лише два місяці, це стало важливим кроком до вирішення проблеми дефіциту донорських органів.
Боротьба з інфекційними захворюваннями. CRISPR-системи розробляють як «антибіотики нового покоління», здатні вибірково знищувати патогенні бактерії, не зачіпаючи корисну мікрофлору. Також досліджується можливість використання генного драйву для контролю популяцій комарів — переносників малярії та лихоманки денге.
Персоналізована медицина. У перспективі CRISPR може стати основою для індивідуальних терапій, розроблених під конкретного пацієнта та його унікальний набір мутацій.
Ключові факти про CRISPR
| Факт | Деталі |
|---|---|
| Рік відкриття структури CRISPR | 1987 (Йосідзумі Ішино, Японія) |
| Рік створення інструменту CRISPR/Cas9 | 2012 (Шарпентьє та Дудна) |
| Нобелівська премія | 2020, хімія (Шарпентьє та Дудна) |
| Перший схвалений препарат | Casgevy (exa-cel), 2023 |
| Кількість клінічних випробувань | Понад 80 (станом на 2025 рік) |
| Вартість базового набору | Від $30–50 за одну мішень |
| Точність | Здатний знайти 1 послідовність серед 3 млрд пар нуклеотидів |
Чому CRISPR важливий для кожного
CRISPR — це не просто лабораторний інструмент. Це технологія, яка вже змінює медицину, сільське господарство та фундаментальну науку. Вона ставить перед людством питання, відповіді на які визначать наше майбутнє.
Чи зможемо ми перемогти генетичні захворювання? Як зміниться продовольча безпека? Де межа між лікуванням та «покращенням» людини? Ці питання стосуються кожного з нас, незалежно від того, наскільки ми далекі від біології.
Одне можна сказати напевно: CRISPR — це одне з найважливіших наукових відкриттів XXI століття. І його вплив на наше життя буде лише зростати.