- Що таке CRISPR/Cas9 і як він працює
- Плюси та переваги CRISPR/Cas9
- Висока точність редагування
- Простота та доступність
- Універсальність застосування
- Потенціал у лікуванні генетичних захворювань
- Прискорення наукових досліджень
- Революція в сільському господарстві
- Порівняння CRISPR/Cas9 з іншими методами редагування геному
- Мінуси та недоліки CRISPR/Cas9
- Офф-таргет ефекти (нецільові мутації)
- Проблема доставки в клітини
- Невідомі довгострокові наслідки
- Етичні дилеми
- Патентні суперечки та регуляторні бар’єри
- Ризик біологічної зброї
- Зведена таблиця: плюси та мінуси CRISPR/Cas9
- Майбутнє технології CRISPR/Cas9
- Нові покоління CRISPR-систем
- Перспективні напрямки досліджень
- Часті запитання (FAQ)
- Чи безпечне редагування геному CRISPR/Cas9 для людини?
- Скільки коштує CRISPR-терапія?
- Чим CRISPR/Cas9 відрізняється від ГМО?
- Які захворювання вже лікують за допомогою CRISPR?
- Чи можна за допомогою CRISPR створити «суперлюдину»?
- Чи легально редагування геному в Україні?
- Висновки
Технологія CRISPR/Cas9 — це метод точкового редагування ДНК, який дозволяє вченим видаляти, вставляти або замінювати конкретні ділянки генетичного коду. Систему вперше описали Дженніфер Дудна та Еммануель Шарпентьє у 2012 році, а вже у 2020 вони отримали за це Нобелівську премію з хімії.
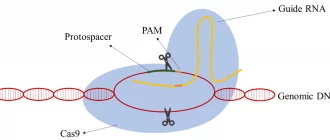
За принципом дії CRISPR/Cas9 нагадує «молекулярні ножиці». Спеціальна направляюча РНК знаходить потрібну ділянку ДНК, а білок Cas9 розрізає подвійну спіраль саме в цьому місці. Далі клітина або «зшиває» розрив самостійно, або вчені вставляють нову послідовність нуклеотидів.
Сьогодні CRISPR/Cas9 застосовують у медицині, сільському господарстві, біотехнологіях та фундаментальній науці. Проте разом із величезними перевагами технологія несе й серйозні ризики — від непередбачуваних мутацій до етичних дилем. Розберемо детально плюси та мінуси редагування геному.
Що таке CRISPR/Cas9 і як він працює
CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats) — це природний механізм імунного захисту бактерій. Бактерії використовують його, щоб «запам’ятовувати» ДНК вірусів і знищувати їх при повторному зараженні. Вчені адаптували цей механізм для цілеспрямованого редагування генів будь-якого організму.
Процес складається з трьох ключових етапів:
- Розпізнавання — направляюча РНК (gRNA) сканує ДНК і знаходить цільову послідовність довжиною 20 нуклеотидів
- Розрізання — білок-нуклеаза Cas9 створює двониткові розриви в обох ланцюгах ДНК
- Репарація — клітина «ремонтує» розрив шляхом негомологічного з’єднання кінців (NHEJ) або гомологічної рекомбінації (HDR)
Саме на етапі репарації вчені можуть вимкнути ген (нокаут), виправити мутацію або вставити нову послідовність. Це робить CRISPR/Cas9 надзвичайно універсальним інструментом.
Факт: Станом на 2025 рік у світі зареєстровано понад 70 клінічних випробувань із застосуванням CRISPR-терапії. У грудні 2023 року FDA та MHRA схвалили перший CRISPR-препарат — Casgevy (екзагамглоген автемсел) — для лікування серповидноклітинної анемії та бета-таласемії.
Плюси та переваги CRISPR/Cas9
Технологія CRISPR/Cas9 відкрила нову еру в генетичній інженерії. Її переваги охоплюють медицину, сільське господарство, промисловість та фундаментальну науку. Розглянемо основні плюси детально.
Висока точність редагування
CRISPR/Cas9 дозволяє змінювати геном із точністю до одного нуклеотиду. Направляюча РНК розпізнає цільову ділянку ДНК довжиною 20 «літер», що забезпечує високу специфічність. Це принципово відрізняє метод від попередніх технологій — ZFN та TALEN, — де точність була значно нижчою.
Нові модифікації системи, зокрема base editing (редагування основ) та prime editing (прайм-редагування), підвищили точність ще більше. Вони дозволяють замінювати окремі нуклеотиди без створення двониткових розривів, що мінімізує ризик небажаних мутацій.
Простота та доступність
Порівняно з попередніми методами генної інженерії, CRISPR/Cas9 значно простіший у використанні. Для створення нової направляючої РНК потрібно лише синтезувати коротку послідовність нуклеотидів. Це займає кілька днів і коштує від 50 до 200 доларів за один експеримент.
Для порівняння: розробка одного ZFN-конструкту могла коштувати 5 000–25 000 доларів і займала тижні. Така доступність демократизувала генетичні дослідження — тепер навіть невеликі лабораторії можуть працювати з редагуванням геному.
Універсальність застосування
CRISPR/Cas9 працює практично в будь-якому типі клітин та організмів. Технологію успішно застосовують у:
- Бактеріях та дріжджах — для промислової біотехнології та виробництва ферментів
- Рослинах — для створення стійких до посухи, шкідників та хвороб сортів
- Тваринах — для моделювання захворювань та створення трансгенних організмів
- Клітинах людини — для генної терапії та дослідження механізмів хвороб
Ця універсальність робить CRISPR/Cas9 ключовим інструментом сучасної біології.
Потенціал у лікуванні генетичних захворювань
Найбільш вражаючий потенціал CRISPR/Cas9 — у лікуванні спадкових хвороб. Технологія дозволяє виправляти мутації безпосередньо в ДНК пацієнта, усуваючи причину захворювання, а не лише його симптоми.
Активні клінічні дослідження вже ведуться для таких захворювань:
- Серповидноклітинна анемія — перший схвалений CRISPR-препарат Casgevy (2023)
- Бета-таласемія — також схвалено лікування Casgevy
- Транстиретиновий амілоїдоз — клінічні випробування NTLA-2001 від Intellia Therapeutics
- Спадковий ангіоневротичний набряк — фаза II клінічних випробувань
Крім того, дослідники працюють над CRISPR-терапією для лікування м’язової дистрофії Дюшенна, муковісцидозу та деяких форм вродженої сліпоти.
Прискорення наукових досліджень
До появи CRISPR/Cas9 створення генетично модифікованої миші займало 1–2 роки. Тепер цей процес можна завершити за кілька тижнів. Це кардинально прискорило дослідження в галузі онкології, нейробіології та імунології.
Вчені використовують CRISPR-скринінг для одночасного аналізу тисяч генів. Наприклад, методом CRISPR-скринінгу було ідентифіковано гени, відповідальні за стійкість ракових клітин до хіміотерапії. Це відкриває шлях до розробки нових протиракових препаратів.
Революція в сільському господарстві
CRISPR/Cas9 дозволяє створювати нові сорти рослин без вбудовування чужорідних генів. Це принципово відрізняє технологію від класичних ГМО. У багатьох країнах CRISPR-відредаговані рослини не підпадають під регуляцію ГМО, що спрощує їх комерціалізацію.
Приклади успішних розробок:
- Помідори з підвищеним вмістом GABA — вже продаються в Японії (Sanatech Seed)
- Пшениця зі зниженим вмістом глютену — для людей із целіакією
- Рис, стійкий до бактеріального опіку — для забезпечення продовольчої безпеки
Порівняння CRISPR/Cas9 з іншими методами редагування геному
Щоб краще зрозуміти переваги CRISPR/Cas9, порівняємо його з попередніми технологіями генної інженерії.
| Параметр | CRISPR/Cas9 | TALEN | ZFN |
|---|---|---|---|
| Вартість | 50–200 $ | 500–5 000 $ | 5 000–25 000 $ |
| Час розробки | Кілька днів | Кілька тижнів | Кілька місяців |
| Точність | Висока | Висока | Середня |
| Мультиплексність | Так (кілька генів одночасно) | Обмежена | Ні |
| Простота дизайну | Проста (синтез РНК) | Складна (білкова інженерія) | Дуже складна |
| Офф-таргет ефекти | Помірні (знижуються) | Низькі | Помірні |
Як видно з таблиці, CRISPR/Cas9 перевершує попередні методи за більшістю параметрів. Головна перевага — поєднання низької вартості, простоти та можливості одночасного редагування кількох генів.
Мінуси та недоліки CRISPR/Cas9
Попри революційний потенціал, технологія CRISPR/Cas9 має суттєві обмеження. Деякі з них є технічними і вирішуються з часом, інші — фундаментальними та етичними.
Офф-таргет ефекти (нецільові мутації)
Офф-таргет ефекти — це ненавмисні зміни ДНК у ділянках, які не були цільовими. Направляюча РНК може «помилитися» і зв’язатися з ділянкою, схожою на цільову, що призведе до небажаних мутацій.
Дослідження 2023 року, опубліковане в журналі Nature Biotechnology, показало, що деякі офф-таргет мутації можуть виникати з частотою до 1–5% залежно від дизайну направляючої РНК. Це особливо критично для клінічного застосування, де навіть одна помилкова мутація може спричинити онкологічне захворювання.
Для зниження ризику вчені розробляють:
- High-fidelity Cas9 — модифіковані варіанти білка зі зниженою офф-таргет активністю
- Cas12a та Cas13 — альтернативні нуклеази з іншим профілем специфічності
- Anti-CRISPR білки — «вимикачі» системи для обмеження часу дії
Проблема доставки в клітини
Навіть ідеально спроєктована CRISPR-система марна, якщо її не вдається доставити в потрібні клітини. Це одна з найбільших технічних перешкод для клінічного застосування.
Основні методи доставки та їхні обмеження:
| Метод доставки | Переваги | Обмеження |
|---|---|---|
| Аденоасоційовані віруси (AAV) | Ефективна доставка, низька імуногенність | Обмежений розмір вантажу (~4,7 кб), Cas9 занадто великий |
| Ліпідні наночастинки (LNP) | Немає обмеження розміру, тимчасова експресія | Переважно потрапляють у печінку, складно таргетувати інші органи |
| Електропорація | Висока ефективність ex vivo | Не підходить для in vivo доставки |
| Рибонуклеопротеїнові комплекси (RNP) | Тимчасова дія, менше офф-таргет ефектів | Складність масштабування виробництва |
Особливо складно доставити CRISPR-компоненти через гематоенцефалічний бар’єр для лікування нейродегенеративних захворювань, а також у м’язову тканину при м’язовій дистрофії.
Невідомі довгострокові наслідки
Технологія CRISPR/Cas9 існує трохи більше десяти років. Цього недостатньо, щоб оцінити довгострокові наслідки генетичних змін, особливо при редагуванні зародкових клітин (germline editing).
Основні побоювання стосуються:
- Мозаїцизму — коли редагування відбувається не у всіх клітинах ембріона, що створює організм із «змішаним» геномом
- Хромотрипсису — масштабних хромосомних перебудов, виявлених у деяких дослідженнях після CRISPR-редагування
- Епігенетичних змін — впливу на регуляцію генів, який може проявитися через покоління
Дослідження 2024 року в Cell показало, що двониткові розриви ДНК, створені Cas9, іноді призводять до великих делецій (втрат ділянок ДНК) розміром до кількох тисяч пар основ. Це значно більше, ніж очікувалося раніше.
Етичні дилеми
Редагування геному людини порушує фундаментальні етичні питання, які суспільство ще не вирішило. Головна лінія розмежування проходить між соматичним та зародковим редагуванням.
Соматичне редагування (зміни в клітинах дорослого організму) — загалом прийнятне з етичної точки зору, оскільки зміни не передаються нащадкам. Саме так працює Casgevy при лікуванні серповидноклітинної анемії.
Зародкове редагування (зміни в ембріонах або статевих клітинах) — викликає гострі дискусії, адже зміни передаються всім наступним поколінням. У 2018 році китайський вчений Хе Цзянькуй створив перших у світі CRISPR-відредагованих дітей, що спричинило міжнародний скандал та його ув’язнення.
Ключові етичні питання:
- «Дизайнерські діти» — ризик використання технології для «покращення» людини, а не лише лікування хвороб
- Соціальна нерівність — генна терапія коштує від 1 до 3,5 мільйонів доларів, що робить її недоступною для більшості
- Інформована згода — майбутні покоління не можуть дати згоду на зміни у своєму геномі
Патентні суперечки та регуляторні бар’єри
Патентна битва між Broad Institute (Фенг Чжан) та Каліфорнійським університетом у Берклі (Дженніфер Дудна) тривала з 2012 по 2022 рік. У 2022 році Патентний суд США визнав пріоритет Broad Institute для застосування CRISPR в еукаріотичних клітинах.
Ця невизначеність ускладнює комерціалізацію. Компанії мають отримувати ліцензії від різних патентовласників, що збільшує вартість розробки та уповільнює впровадження нових терапій.
Регуляторне середовище також залишається фрагментованим:
- ЄС — CRISPR-відредаговані організми прирівнюються до ГМО (суворе регулювання)
- США — більш ліберальний підхід, CRISPR-рослини без чужорідної ДНК не регулюються як ГМО
- Японія — перша країна, що дозволила продаж CRISPR-відредагованих продуктів (2021)
Ризик біологічної зброї
Доступність та простота CRISPR/Cas9 створюють ризики у сфері біобезпеки. Теоретично технологію можна використати для створення більш вірулентних патогенів або модифікації організмів із непередбачуваними наслідками.
У 2016 році директор Національної розвідки США Джеймс Клеппер включив генне редагування до списку потенційних загроз масового ураження. Міжнародне наукове співтовариство активно працює над протоколами біобезпеки, але універсальних механізмів контролю поки не існує.
Зведена таблиця: плюси та мінуси CRISPR/Cas9
| Плюси | Мінуси |
|---|---|
| Висока точність редагування (до 1 нуклеотиду) | Офф-таргет ефекти (нецільові мутації 1–5%) |
| Низька вартість (50–200 $ за експеримент) | Складність доставки в деякі типи клітин |
| Простота та швидкість розробки | Невідомі довгострокові наслідки |
| Універсальність (працює в будь-яких організмах) | Етичні дилеми (зародкове редагування) |
| Лікування спадкових захворювань (Casgevy) | Патентні суперечки та регуляторна невизначеність |
| Прискорення наукових досліджень у рази | Ризики біобезпеки та подвійного використання |
| Революція в сільському господарстві | Висока вартість клінічного застосування (1–3,5 млн $) |
Майбутнє технології CRISPR/Cas9
Технологія CRISPR/Cas9 стрімко розвивається. Нові модифікації системи вирішують багато поточних обмежень, а сфери застосування постійно розширюються.
Нові покоління CRISPR-систем
Base editing (редагування основ), розроблене лабораторією Девіда Лю у 2016 році, дозволяє замінювати одну «літеру» ДНК на іншу без розрізання подвійної спіралі. Це суттєво знижує ризик офф-таргет ефектів та великих делецій.
Prime editing (прайм-редагування, 2019) — ще точніший метод, який може виконувати всі 12 типів точкових мутацій, а також невеликі вставки та делеції. Його називають «пошук і заміна» для ДНК.
Epigenome editing — модифікований Cas9 без нуклеазної активності (dCas9) використовується для вмикання або вимикання генів без зміни послідовності ДНК. Це відкриває шлях до зворотного редагування геному.
Перспективні напрямки досліджень
- Ксенотрансплантація — редагування геному свиней для трансплантації органів людям (компанія eGenesis)
- Генний драйв — модифікація комарів для боротьби з малярією (Target Malaria)
- Онкологія — CRISPR-модифіковані CAR-T клітини для лікування раку
- Антибіотикорезистентність — CRISPR-фаги для знищення стійких бактерій
Часті запитання (FAQ)
Чи безпечне редагування геному CRISPR/Cas9 для людини?
Соматичне редагування (зміни в клітинах дорослого організму) вважається відносно безпечним при дотриманні протоколів. Перший схвалений CRISPR-препарат Casgevy пройшов ретельні клінічні випробування. Проте ризики офф-таргет мутацій та довгострокових наслідків залишаються предметом досліджень. Зародкове редагування (зміни в ембріонах) наразі заборонене у більшості країн через невідомі ризики.
Скільки коштує CRISPR-терапія?
Лабораторний експеримент із CRISPR/Cas9 коштує від 50 до 200 доларів. Проте клінічне застосування значно дорожче. Наприклад, лікування Casgevy оцінюється приблизно в 2,2 мільйони доларів за курс. Вартість зумовлена складністю виробництва, клінічних випробувань та індивідуальним підходом до кожного пацієнта.
Чим CRISPR/Cas9 відрізняється від ГМО?
Класичні ГМО містять чужорідні гени з інших організмів (трансгенез). CRISPR/Cas9 може вносити зміни, аналогічні природним мутаціям, без вбудовування чужорідної ДНК. Тому у багатьох країнах (США, Японія, Аргентина) CRISPR-відредаговані організми без чужорідних генів не класифікуються як ГМО.
Які захворювання вже лікують за допомогою CRISPR?
Станом на 2025 рік офіційно схвалено CRISPR-терапію для двох захворювань: серповидноклітинної анемії та бета-таласемії (препарат Casgevy). Клінічні випробування тривають для транстиретинового амілоїдозу, спадкового ангіоневротичного набряку, ВІЛ-інфекції та деяких форм раку.
Чи можна за допомогою CRISPR створити «суперлюдину»?
Теоретично CRISPR/Cas9 може змінювати гени, пов’язані з фізичними та когнітивними характеристиками. Проте на практиці більшість таких ознак (інтелект, зріст, атлетизм) контролюються сотнями генів та залежать від середовища. Сучасний рівень знань не дозволяє «запрограмувати» складні ознаки. Крім того, зародкове редагування для «покращення» людини заборонене міжнародними конвенціями.
Чи легально редагування геному в Україні?
В Україні немає спеціального законодавства, що регулює CRISPR/Cas9. Дослідження з генетичною модифікацією підпадають під загальне законодавство про ГМО (Закон України «Про державну систему біобезпеки при створенні, випробуванні, транспортуванні та використанні генетично модифікованих організмів»). Клінічне застосування генної терапії регулюється МОЗ України.
Висновки
CRISPR/Cas9 — це, безперечно, одне з найважливіших наукових відкриттів XXI століття. Технологія вже змінила підхід до лікування генетичних захворювань, прискорила наукові дослідження та відкрила нові можливості в сільському господарстві.
Водночас залишаються серйозні виклики: офф-таргет ефекти, проблеми доставки, етичні дилеми та регуляторна невизначеність. Ці обмеження не знецінюють технологію, а вказують на напрямки, де потрібна подальша робота.
Баланс між потенціалом та ризиками CRISPR/Cas9 визначатиме майбутнє не лише генетичної інженерії, а й медицини, сільського господарства та суспільства в цілому. Відповідальний підхід до розвитку та регулювання цієї технології — запорука того, що її переваги будуть реалізовані на благо людства.